Positronemmisionstomografi är en visualiseringsteknik som kräver en omfattande teknologisk infrastruktur. I Åbo samarbetar Åbo Akademi, Åbo universitet och Åbo universitetscentralsjukhus kring verksamheten och utvecklandet av det nationella PET-centret.
Text: Marcus Prest
PET-centrets hjärta partikelacceleratorn, cyklotronen, finns nere i källarvåningen bakom en sju ton tung strålningssäker dörr i ett stenhus bakom universitetssjukhusets huvudbyggnad. Utrymmet är avspärrat medan tillverkningen av isotoper pågår. Produktionen hålls igång fem dagar i veckan – isotoperna är högradioaktiva. De används för forskning och inom den medicinska forskningen, till exempel för cancerdiagnoser – en verksamhet som pågår i våningarna ovanför acceleratorlaboratoriet.
PET-centrets hjärta partikelacceleratorn, cyklotronen.Cyklotronen körs från ett manöverbord som övervakas av laboratieingenjör Stefan Johansson (Åbo Akademi) och forskare Johan Rajander (Åbo Åkademi). Det tre isotoper som i huvudsak produceras är kol-11, fluor-18 och koppar-64. Produktionen av radioaktiva isotoper är acceleratorlaboratoriet vid Åbo Akademis ansvar, medan radiokemin, det vill säga förenandet av isotoperna med molekyler som för isotoperna till rätt receptorer i människokroppen är Åbo universitets ansvar. Diagnostiseringen görs av Åbo universitetssjukhus.
Cyklotronen är en form av partikelaccelerator som med hjälp av magnetfält och en högfrekvent växelspänning skapar högenergetiska partiklar av joner som kontrollerat leds ut ur magnetfältet och bildar en jonstråle. Cyklotronen och dess stråltransport system har tillverkats av Efremovinstitutet i Sankt Petersburg, medan resten av produktionssystemet och transportlinjerna är tillverkat av experterna på PET-centret.
– Vi utvecklar och tillverkar själv target-systemen, eller strålmålskamrarna, säger Stefan Johansson.
Strålmålskamrarna är massiva boxar i aluminium med exakta gångar för jonstrålen och och utrymmen för själva strålmålen. Åbo Akademi har en egen metallverkstad där man arbetar med aluminiumdelarna.
– De två produkter som tillverkas mest är kol-11 och fluor-18. Kol och fluor kräver olika typer av strålmål, säger Johan Rajander.
Produktionen och tillämpning av isotopen kol-11 går förenklat till så här: Cyklotronen skjuter ut en jonstråle, i detta fall protoner, med en energi på 18 MeV (miljoner elektronvolt) som styrs och fokuseras in i ett strålmål där strålen träffar en gas med högt tryck – en blandgas av kväve och en procent syre vid cirka 40 atmosfärers tryck. Trycket är anpassat till strålmålets längd – olika tryck ger olika täthet – vilket inverkar på protonstrålens räckvidd i gasen. När protonerna träffar kvävgasen sprider strålen ut sig vilket förklarar strålmålskammrarnas koniska form. Samtidigt uppstår en kärnreaktion; en proton in i atomkärnan – en alfapartikel ut. Kol-11 är en radioaktiv isotop med en halveringstid på 20,4 minuter. Efter bestrålningen skickas den bestrålade gasen upp till blyskåpen i radiokemilaboratoriets renutrymme på andra våningen och isotopen förenas med rätt typ av molekyl och ”förädlas” till ett injicerbart preparat, ett radioläkemedel. Radioläkemedlet ges som en injektion till en väntande patient som sedan skickas till PET-undersökning där läkare genom PET-skannern avläser strålningen som härstammar från den skräddarsydda molekylen. Kol-11 och fluor-18 sönderfaller via positronemission, en speciell form av så kallad radioaktivt betasönderfall.
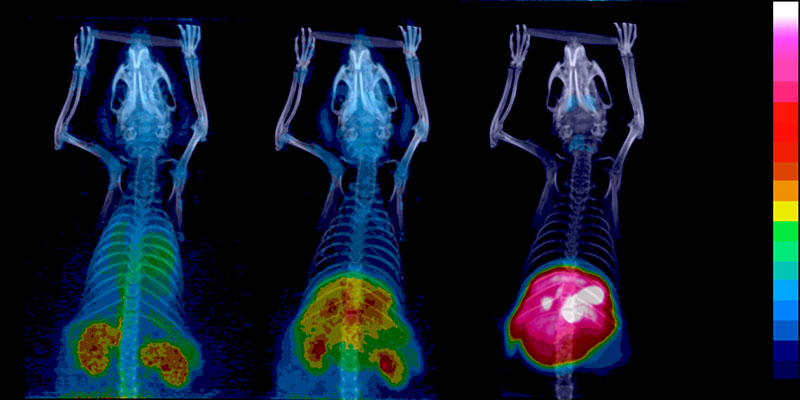
– När positronerna, som härstammar från det radioaktiva sönderfallet träffar elektroner uppstår en annihilation och två gammakvanta, fotoner, rör sig åt motsatt håll – vilket är en händelse som detekteras i en PET-skanner. Det är en tydlig radioaktiv signal. Man får alltså en bra bild, säger doktor Sarita Forsback, från Åbo universitet.
De radioaktiva preparaten är kortlivade mediciner, man måste tillverka nya varje dag och en stor del av Forsbacks tid går åt till att kontrollera att alla tidtabeller stämmer med koordination av acceleratorkörningar (så att rätt produkt tillverkas vid rätt tid), arbete vid blyskåpen, och att rätt patient är förberedd när preparatet är klart och att relevant personal är klar vid PET-skannern.
– Det som känns är ansvaret för helheten, säger Forsback.
De här preparaten är inte som Burana. Isotoperna är radioaktiva och allt arbete med dem måste göras i blyskåp, varje omgång måste kvalitetsbestämmas och skräddarsys för patienten.
– Varje ny typ av radioläkemedel vi tagit fram och varje del i systemet i framställningsprocessen måste gå igenom en väldigt noggrann gallring innan de tas i bruk. FIMEA, det vill säga säkerhets- och utvecklingscentret för läkemedelsområdet kollar oss ständigt.
De radioaktiva preparaten kallas mediciner trots att de inte har någon läkande effekt. I själva verket är det mycket viktigt att de inte har någon effekt alls. Den stora fördelen med radiokemin är att man kan undersöka patienter, positionera tumörer även i svårtåtkomliga organ, bestämma om tumörerna är hypoxiska (om de använder syre – vilket betyder att strålningsbehandling fungerar sämre) – utan att behöva använda kirurgi. Med hjälp av skanningen kan man också i viss grad bestämma vilken art av tumör man har att göra med, vilket betyder att man kan göra mera exakta behandlingsprogram.
– Molekylerna är skräddarsydda så att de har en hög affinitet för en specifik process i människan. De samlas i de receptorer vi söker, utan att påverka receptorernas funktion. En stor del av utvecklingsarbetet vi gör inom radiokemin är att hitta sätt att få radioaktiva isotoper att sluta sig till rätt typ av molekyl.
Det mest använda radioläkemedlet i PET undersökningar är FDG – fluorodeoxyglukos tillverkas genom att fästa isotopen fluor-18 på en glukosmolekyl. FDG är kommersiellt tillgängligt men PET-centret i Åbo tillverkar den själv.
– FDG fungerar på de flesta tumörer eftersom tumörer tenderar att använda mycket snabb energi, det vill säga socker. Det gör att FDG, som alltså är en glukosanalog, socker med en radioaktiv isotop, söker sig till tumören som förbränner socker intensivare än andra vävnader. Eftersom koncentrationen av FDG då kommer att bli större i tumörvävnaden kommer vi också att se mera gammastrålning från annihilationen av positroner från FDG som träffar elektronerna i tumörens massa.
– För radiokemiska inmärkningar använder vi en i Åbo utvecklad metod som är unik i världen. Den baserar sig på en elektrisk urladdning som upplöser alla bindningar i molekylen. Istället för att alltid få en negativt laddad fluor-18-jon, kan vi också skapa positivt laddade fluor-18-joner som ger oss flera kombinationsmöjligheter. Dessutom är processen både snabb, automatiserad och ger ofta radioläkemedel som har mycket fördelaktiga egenskaper för avbildning.
Sarita Forsback har i arbetet med sin doktorsavhandling själv utvecklat två nya typer av molekyler som ansluter sig till dopaminreceptorer. Molekylerna är användbar i till exempel forskningen kring Parkinsons sjukdom.
Åbo PET-center
Åbo PET-center grundades på 1970-talet. Centret fick status som nationellt forskningsinstitut 1996. Centret framställer och forskar i kortlivade isotoper som avger positronstrålning – verksamheten är underställd medicinsk forskning av diagnostisering av patienter genom radiokemi.
PET-centrets kärnverksamhet grundar sig på en överenskommelse mellan Åbo Akademi, Åbo universitet och Åbo universitetscentralsjukhus. Hela verksamheten är förlagd till universitetscampus och sjukhusområdet. Centret består av acceleratorlaboratoriet, radiofarmakologiska kemilaboratoriet, prekliniska undersökningslaboratoriet och PET-laboratoriet. Centret anställer för tillfället fler än 110 personer som inkluderar personal och forskare från olika forskningsområden. PET-centret har tre stycken cyklotroner, 19 hot cells (för tracerproduktion) och sex PET eller PET/CT skannrar och digitala ultraljudssystem.
Centret har två huvudsakliga uppgifter: att producera högkvalitativ forskning och att tillhandahålla diagnostiseringstjänster för hela landet. Forskningen vid PET-centret koncentrar sig kring fyra huvudområden: cellens energimetabolism, neurotransmission, preklinisk visualisering och radiokemisk forskning. Samarbetet mellan universiteten och läkemedelsindustrin är aktivt.
Radioaktiv strålning
Tillverkningen av radioaktiva isotoper innebär att omgivningen där de tillverkas utsätts för radioaktiv strålning – därför är cyklotronen och strålmålen instängda bakom flera meter tjocka betongväggar som absorberar den radioaktiva strålningen. De isotoper som tillverkas i acceleratorlaboratoriet har dock en snabb halveringstid, det vill säga de förlorar hälften av sin radioaktivetet under en halveringstid (kol-11 20,4 minuter, F-18 109,7 minuter och koppar-64 12,7 timmar) varefter de igen förlorar hälften av hälften, tills strålningen har försvunnit. Det gör materialen säkra både för personalen och för patienten, men å andra sidan blir användningstiden kritisk eftersom en isotop inte kan vänta länge på en patient. Radioaktiviteten i kol-11 halveras på 20,4 minuter – det betyder att isotopen måste injiceras i blodcirkulationen på den väntande patienten och patienten skannas inom ungefär en timme för att få en bra bild från en PET-scanner. Fluor-18 som används i bland annat FDG har en halveringstid på 109,7 minuter.
– En del besökare vågar inte komma in och titta på cyklotronen, säger Stefan Johansson.
– Det som få känner till är att man blir utsatt för mera strålning på ett interkontinentalt flyg än här inne i labbet, säger Johan Rajander.
Strålning är ett område som väcker ett instinktivt obehag hos många. De förhöjda strålningsnivåerna som rapporterades efter Fukushimakatastrofen väckte oro över hela världen.
– Ändå var den strålning som uppmättes till exempel i Tokyo (cirka 240 kilometer från Fukushima) knappt högre än den genomsnittliga bakgrundsstrålningen i Helsingfors, säger Rajander.