Ett konsortium lett av datavetenskapen vid ÅA söker vägar att bedriva cancerforskning med hjälp av de massiva mängder patientdata som finns lagrade i databanker tillhörande de olika cellforskningslabben i världen.
Text & foto: Marcus Prest
PATIENTDATA SAMLAS in varje dag. En hel del värdefull information finns i databankerna. Nu försöker datavetarna hitta ett sätt att utnyttja informationen i cancerforskningen.
Det nu aktuella projektet, som heter Network pharmacology: drug re-purposing and discovery of multi-drug therapies by analytical approaches har sina rötter i ett Finland Akademi-projekt i syntetisk biologi som påbörjades 2013.
Det underliggande projektet byggde på grundforskning i matematik för att utveckla räkneverktyg för att hjälpa till i designen av nya läkemedel. Verktygen kommer från matematik, datavetenskap och molekylärbiologi. I samband med det bildades en koncern bestående av Åbo Akademi, Institutet för molekylärmedicin i Finland (FIMM), Åbo universitet och Imperial College i London. Det aktuella projektet hör ihop med att Tekes genomgått och genomgår en mängd förändringar, främst nedskärningar.
– En följd av förändringarna och nedskärningarna, som för en gångs skull inte är negativ, är att Tekes nu söker sätt att försnabba processen som bär från forskning vid universiteten till tillämpningar i näringslivet, säger Ion Petre, professor i datavetenskap vid Åbo Akademi.
– Det är inte det som är positivt, det positiva är att man – tvärtemot hur man gjort tidigare – nu först frågat universiteten, bett oss se över vår forskning och se vad vi har som kunde utvecklas för marknaden inom en rimlig tid, istället för att fråga näringslivet vad de önskar sig och sedan försöka beställa det näringslivet vill ha från universiteten.
Petres grupp hade inget som de ansåg att på en tillräckligt kort tid kunde förvandlas till något marknadsmässigt intressant. De nämnde ändå den kompetens de hade skaffat genom det nämnda projektet i syntetisk biologi och hur den kunskapen eventuellt kunde användas för att starta ett nytt projekt, som använder de stora mängder data som finns inom läkemedelsforskningen och patientdata, för att ur den extrahera relevanta data för tillverkningen av nya precisa mediciner.
– Idén gillades och vi tilldelades pengar för ett kort projekt från juni till november ifjol för att gå vidare.
Petres grupp vid Åbo Akademi bildade ett konsortorium, den här gången med Orion Pharma, Misvik Biology (spinn-off från VTT), Medisapience (också en VTT-spinn-off) och Euformatics. Samtliga bolag är finländska. Projektet leds av professor Petre och Eugen Czeizler, forskare vid Åbo Akademis datavetenskap.
– Projektet handlar om cancerforskning, med utgångspunkt i att se på cancer som ett slags ”systemsjukdom” som uppstår i interaktioner inuti cellen. Ett av grundproblemen är att man inte vet exakt vart i cellen man ska rikta in sig i bekämpandet av en specifik form av cancer och ett följdproblem är att man inte vet hur man ska nå den del av DNA:t som man vill åt om man lyckas få reda på vart man borde rikta sig. Vår idé är att närma oss frågan ur ett systematiskt perspektiv, säger Petre.
– Det här hänger ihop med lanseringen av CRISPR-Cas9 – en genomredigeringsteknologi som utvecklades för två år sedan vid Harvard University och MIT. Forskarna som tog fram det här kommer nästan säkert att tilldelas Nobelpris inom kort.
CRISPR-Cas9, som varit mycket på tapeten på sistone, förvandlar biologi till ingenjörsvetenskap. När det gäller cancerforskning visar CRISPR att det finns vissa specifika gener som är centrala för specifika typer av cancer. Det går att stänga av dessa gener om man går in i cellen väldigt exakt. Ett av de stora problemen är att läkemedlen är för inexakta, de går in på fel gener. Och man vet inte exakt vilket ämne som når till rätt gen.
Petres grupp såg att deras öppning som datavetenskapare låg i att hitta kunskap om hur man kommer åt de relevanta generna. Man hoppas kunna samla in alla slags data gällande cancermediciner och hur medicinerna verkat på patienter, från databanker i hela världen där testresultat från världens cellforskningslaboratorier har lagrats. I dessa tester har man inte nödvändigtvis haft ögonen på hur medicinerna påverkar specifika gener, men man har registrerat de allmänna effekterna eller andra specifika effekter och utgående från den redan insamlade informationen kan man med rätt kunskap läsa av på vilka gener olika läkemedel fungerat.
Utgående från den informationen kan man hitta fall där läkemedel fungerat på sätt som är intressanta för den nu aktuella forskningen.
– Det här skulle vara ett sätt att ge läkemedelsbolagen bättre chanser till kvalificerade gissningar och förkorta processen i att hitta de specifika ämnen som behövs för att komma åt specifika gener. Allt som gör den processen snabbare och billigare är prioriterat: i nuläget kostar det cirka en miljard euro att utveckla, testa och lansera ett läkemedel vilket bland annat gör villkoren för att finansiera sådan verksamhet ekonomiskt mycket riskabla.
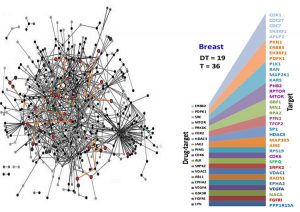
– Vi kommer att bygga nätverk som till exempel kan leda till att man kan ta fram patientspecifik medicin. Vi ska bygga cancernätverk som hittar de rätta generna.
– För mig är det här alltså ett problem som kan lösas utifrån grafer och algoritmer. Jag vet alldeles för lite om cancer och medicin och får inte släppas in i ett labb. Men vad vi har är 15 mycket kompetenta datavetare och ett beräkningsbiologilabb som är state of the art.
De första resultaten i projektet har redan publicerats och mottagits med stort intresse av forskarvärlden. De nya algoritmerna som utvecklats av Petres grupp publicerades vid konferensen Computational Methods in Systems Biology (den primära arenan för metodologisk forskning inom systembiologi) och tilldelades pris för bästa artikel. De första tillämpningarna av algoritmerna har accepterats för publikation av Nature Scientific Reports. Petre säger att fler resultat är på väg.
CRISPR-Cas9 är beteckningen på en genediteringsteknologi. CRISPR står för Clustered Regularly Interspaced Short Palindromic Repeats. Cas9 är namnet på ett enzym.
CRISPR-Cas9-teknologin kan användas för att söka upp specifika delar av den genetiska koden och påverka DNA:t på specifika punkter, till exempel genom att stänga av en muterad (skadad) del av DNA:t, som om den tillåts att fortsätta reproducera sig ger upphov till exempel till cancer eller någon annan sjukdom.
Andra versioner av Cas9-enzymen kan aktivera en specifik del av den genetiska koden istället för att stänga av. En del forskare antar att man också kan använda teknologin för att gå in och modifiera ”fel” i DNA:t för att behandla olika former av ärftliga sjukdomar.
Teknologin är ny och kan visa sig medföra radikala förändringar i vad som är möjligt att påverka i den mänskliga arvsmassan, vilket i sin tur kan leda till radikala resultat som främst utforskats i science fiction.